A companhia farmacêutica AstraZeneca anunciou que sua vacina contra a Covid-19, conhecida como a “Vacina de Oxford”, é “altamente eficaz” na prevenção da doença, e que nenhuma hospitalização ou caso severo da doença foram reportados entre os voluntários que participaram dos testes.
A empresa realizou dois estudos, envolvendo quase 23 mil voluntários. No primeiro, chamado COV002, participaram 12.390 pessoas com 18 anos ou mais, que são saudáveis ou tem doenças crônicas estáveis e tem risco elevado de exposição ao vírus. Elas receberam uma meia-dose da vacina AZD1222, seguida de uma dose completa após um mês, ou então duas doses de um placebo. Neste estudo, a vacina teve eficácia de 90%.
O outro estudo, chamado COV003, foi realizado no Brasil com 10.300 participantes também com 18 anos ou mais, que são saudáveis ou tem doenças crônicas estáveis e tem risco elevado de exposição ao vírus. Os participantes receberam duas doses completas da vacina com intervalo de um mês, ou um placebo. A eficácia neste estudo foi de 60%.
Em outubro um médico brasileiro de 28 anos que participou do COV003 morreu de Covid-19. Entretando, foi determinado que a morte não ocorreu devido à complicações da vacina, já que ele fazia parte do grupo que recebeu um placebo, uma vacina contra a meningite.

Eficácia da vacina da AstraZeneca pode chegar a 90%, dependendo da dosagem. Imagem: AstraZeneca/Divulgação
Um conselho independente determinou que os estudos cumpriram seu objetivo de demonstrar proteção contra a Covid-19 após 14 dias ou mais da segunda dose da vacina. Nenhum incidente de segurança sério relacionado à vacina foi confirmado, e a AZD1222 foi “bem tolerada” nos dois regimes de dosagem.
A AstraZeneca afirma que irá preparar imediatamente pedidos de aprovação condicional ou preliminar a autoridades de saúde ao redor do mundo. A empresa irá solicitar inclusão na listagem de medicamentos de uso emergencial da Organização Mundial de Saúde (OMS) para disponibilidade acelerada da vacina em países de baixa renda. Em paralelo, a análise completa dos resultados está sendo enviada para publicação em um jornal científico.
Testes clínicos também estão sendo conduzidos nos EUA, Japão, Rússia, África do Sul, Quênia e América Latina, e há testes planejados para países na Europa e Ásia. No total, a farmacêutica espera até 60 mil participantes em todo o mundo.
A empresa afirma estar “progredindo rapidamente” na produção, com uma capacidade de até 3 bilhões de doses em 2021, se obtiver aprovação das agências reguladoras. A vacina pode ser armazenada, transportada e manuseada em condições normais de refrigeração (2 a 8 graus Celsius) por até seis meses, e administrada usando a infraestrutura de saúde já existente.
Outras vacinas
Várias outras empresas estão desenvolvendo vacinas contra a Covid-19. A Pfizer e a BioNTech afirmam que sua vacina tem eficácia de 95% e solicitaram aprovação junto à FDA, nos EUA, para seu uso emergencial.
Já a Moderna anunciou que sua vacina tem eficácia de 94,5%. “Por aspiração, você gostaria de ver 90%, mas eu não esperava isso. Achei que seria bom, mas 94,5% é muito impressionante”, disse Anthony Fauci, diretor do Instituto Nacional de Alergia e Doenças Infecciosas dos EUA, em entrevista ao New York Times.
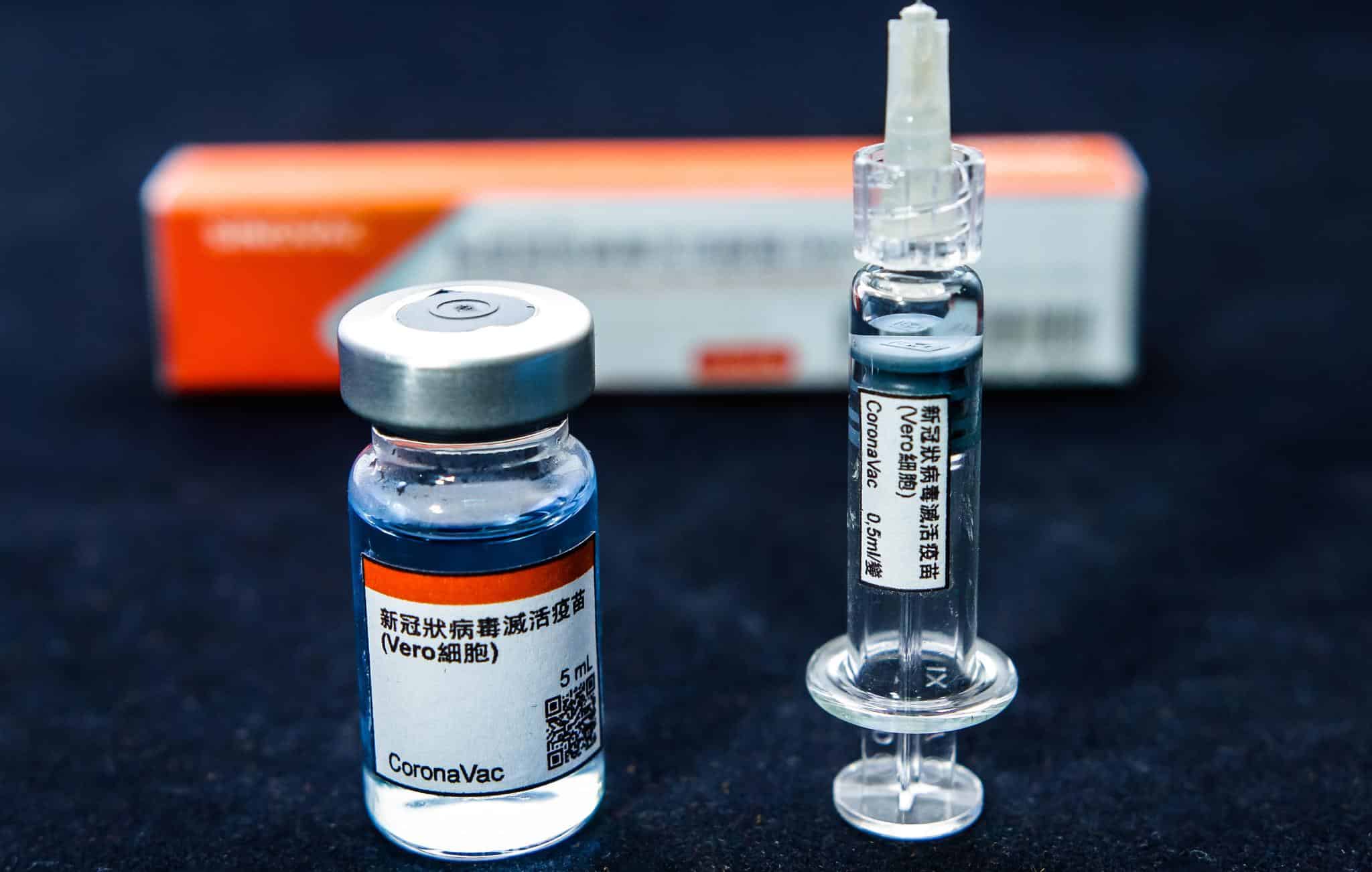
A vacina chinesa Coronavac está em testes em São Paulo. Imagem: cadu.rolim/Shutterstock
Já a chinesa Coronavac, que está sendo testada em São Paulo, teve “98% de eficácia em idosos” segundo o governador do estado, João Doria. Se os resultados forem positivos, o Ministério da Saúde terá 46 milhões de doses disponíveis para vacinação a partir de dezembro. Porém, cada pessoa deve tomar duas doses; sendo assim, 23 milhões de brasileiros poderiam se vacinar nesse momento.
Até maio do próximo ano, o Instituto Butantan poderia produzir 100 milhões de doses da CoronaVac, de acordo com Dimas Covas, presidente do Instituto, desde que receba apoio financeiro do Ministério da Saúde para tal.