Em coletiva nesta segunda-feira (19), o governador de São Paulo, João Doria, precisou rever suas promessas de iniciar a campanha de vacinação contra Covid-19 em 15 de dezembro. Os dados apresentados sobre a CoronaVac ainda não permitiram cravar a eficácia da vacina, embora demonstrem um “alto perfil de segurança”. A resposta definitiva deve chegar até o fim do ano, mas deve inviabilizar a data prevista inicialmente.
Durante apresentação, Dimas Covas, diretor do Instituto Butantan, apresentou apenas os resultados sobre efeitos colaterais com os voluntários no Brasil. Ele revelou que as reações adversas mais comuns foram dor no local da aplicação e, na resposta sistêmica, dores de cabeça foram o efeito colateral mais comum, embora não seja possível cravar que elas tenham sido causadas pela vacina.

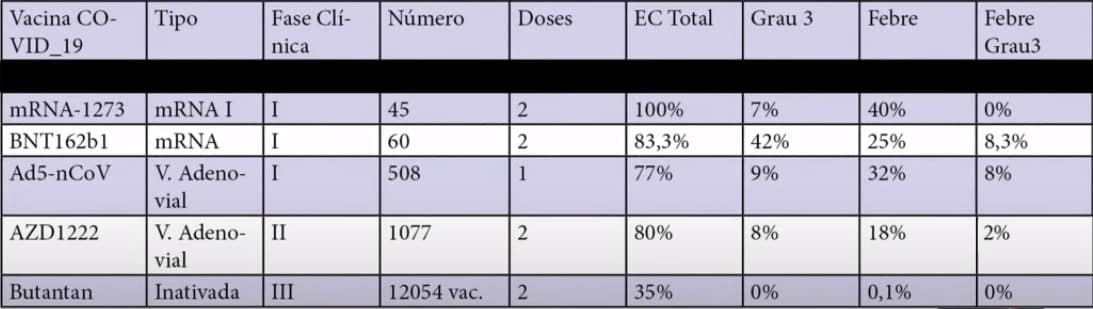
Covas também realizou uma comparação com outras vacinas em fases avançadas de testes, como a da Moderna (mRNA-1273), da Pfizer (BNT162bI), da CanSino (Ad5-nCov) e da AstraZeneca-Oxford (AZD1222). Os números apresentados mostram não só uma incidência inferior de efeitos colaterais, mas uma intensidade mais baixa. Enquanto todas as outras apresentaram alguma reação de grau 3, que é o tipo de evento adverso que impede a pessoa de realizar suas atividades normalmente, embora não chegue a representar um risco à sua vida, a CoronaVac foi a única a registrar, no máximo reações de grau 2.
No entanto, os resultados de segurança, apesar de positivos, não são o que se esperava ver. A expectativa era para os dados sobre a eficácia, mas, ao que tudo indica, ainda não foi alcançado o número mínimo de voluntários infectados para que os pesquisadores possam realizar a análise preliminar dos dados, que permitiria dar entrada no registro na Anvisa e planejar campanhas de vacinação.
O protocolo de pesquisa da CoronaVac prevê a análise interina quando houver 61 casos de contaminação por Covid-19 entre os voluntários, e se uma maioria estatisticamente significante desses casos estiver concentrada no grupo placebo, que recebe apenas uma substância inerte, isso significa que a vacina funciona. No entanto, hoje, esse número ainda não foi alcançado e, como relata Covas, os pesquisadores ainda não sabem o quão distante ele ainda está. Essas informações são sigilosas e acompanhadas apenas por um comitê independente internacional, que não abre quantos casos já estão acumulado ao Butantan.
Existem alguns motivos para que esses números ainda não tenham sido alcançados. Como apresentado durante a coletiva, as taxas de transmissão caíram de forma generalizada no Brasil nas últimas semanas, o que dificulta o passo acelerado dos testes da vacina. Além disso, a oferta de equipamentos de proteção individual para os profissionais de saúde se estabilizou, reduzindo o risco de os voluntários se exporem ao vírus. Para tentar obter os resultados mais rapidamente, os pesquisadores estão procurando mais voluntários, para aumentar as chances de que participantes se infectem.
O Instituto Butantan e o governo de SP sustentam que pedirão o registro da CoronaVac à Anvisa se a pesquisa demonstrar uma eficácia mínima de 50%.