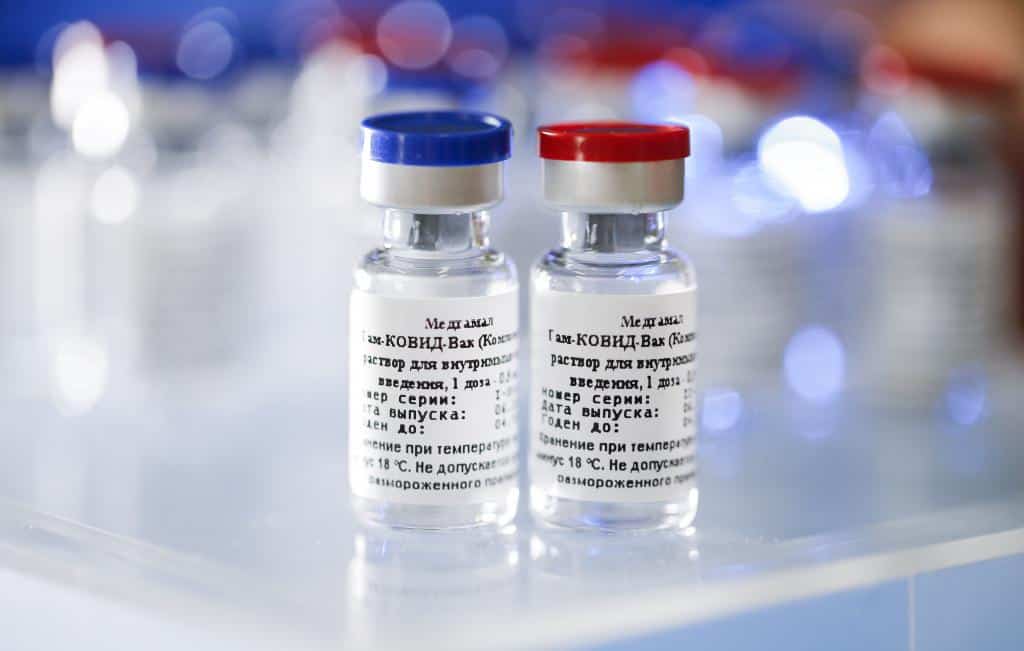
O laboratório que representa a vacina russa Sputnik V no Brasil iniciou um diálogo com a Agência Nacional de Vigilância Sanitária (Anvisa) para a realização de uma pesquisa clínica no País. O pedido formal, porém, ainda não foi realizado.
A única movimentação neste sentido até agora, de acordo com a agência, foi o encaminhamento de documentos prévios por parte do laboratório União Química. Esse contato é parte dos preparativos que precedem a apresentação formal do pedido de pesquisa. A documentação necessária para solicitar a autorização, o Dossiê de Desenvolvimento Clínico de Medicamento (DDCM), porém, não foi enviado.
“Em seu comunicado, o laboratório esclarece que os detalhes para a pesquisa clínica de fase 3 da Sputnik V ainda serão apresentados em data que depende do laboratório”, afirma a Anvisa, em comunicado. “As informações enviadas não são um pedido formal de autorização para a pesquisa e não são suficientes para a autorização da Anvisa’, completa a agência.
O diretor-geral do Fundo Russo de Investimentos Diretos, Kirill Dmitriev, declarou recentemente sua intenção de que a vacina Sputnik V receba a aprovação em diversos países até dezembro – incluindo no Brasil. “No e-mail, o laboratório também manifestou interesse em realizar uma reunião de caráter técnico com a Anvisa antes de pedir formalmente a autorização da pesquisa clínica para a Sputnik V”, explica a agência.

Rússia espera aprovação de Sputnik V em outros países para dezembro. Foto: Divulgação/AFK Sistema
“Acreditamos que já em dezembro poderemos iniciar o fornecimento à América Latina, vamos produzir dezenas de doses de vacina para fornecimentos muito ativos serem iniciados em janeiro”, afirmou Dmitriev na semana passada. Além disso, o executivo explicou que a produção da vacina não será concentrada na Rússia. “Nós confirmamos poder fornecer grandes volumes em dezembro deste ano. Vamos produzi-la no Brasil, Índia, Coreia do Sul, China e em mais um país”, explicou.
Para que isso ocorra, porém, é preciso que o imunizante seja aprovado pelos órgãos reguladores desses países. Se depender da Rússia, isso vai acontecer o mais rápido possível. “Vamos trabalhar com reguladores para que sejamos aprovados rapidamente em seus países”, acrescentou Dmitriev.
Via: Agência Brasil